Selecionada por nossa IA preditiva, esta elétrica já dispara +15% em 2 meses
Introdução e contexto de mercado
A Summit Therapeutics (NASDAQ:SMMT) apresentou sua teleconferência de resultados do 3º tri de 2024 em 30 de outubro de 2024, destacando avanços clínicos significativos para seu composto principal, o ivonescimab, um novo anticorpo biespecífico PD-1/VEGF. As ações da empresa têm mostrado forte desempenho, com dados fundamentais indicando um aumento de 2,65% para US$ 27,07 em 1º de agosto de 2025, e uma variação de 52 semanas de US$ 8,88 a US$ 36,91, refletindo a confiança dos investidores no pipeline da empresa.
Resumo executivo
A Summit Therapeutics reportou uma perda líquida GAAP de US$ 56,3 milhões para o 3º tri de 2024, uma melhora em relação à perda de US$ 60,4 milhões no 2º tri de 2024. A empresa mantém uma forte posição de caixa de US$ 487 milhões em 29 de outubro de 2024, reforçada por uma rodada de financiamento de US$ 235 milhões de importantes investidores de biotecnologia. A apresentação enfatizou resultados clínicos revolucionários para o ivonescimab, particularmente no estudo HARMONI-2, onde demonstrou sobrevida livre de progressão (PFS) superior em comparação com pembrolizumab em câncer de pulmão de células não pequenas (NSCLC) de primeira linha.
Como mostrado na seguinte visão abrangente das conquistas do trimestre:

Destaques do desenvolvimento clínico
O composto principal da Summit, ivonescimab, é posicionado como o único anticorpo biespecífico PD-1/VEGF em Fase III nos territórios licenciados pela empresa, que incluem América do Norte, América do Sul, Japão, Europa, Oriente Médio e África. A empresa possui um extenso programa de desenvolvimento clínico com mais de 25 ensaios clínicos em 17 tipos de tumores, com mais de 1.800 pacientes tratados.
O slide a seguir ilustra a amplitude do programa global de ensaios clínicos da Summit para o ivonescimab:
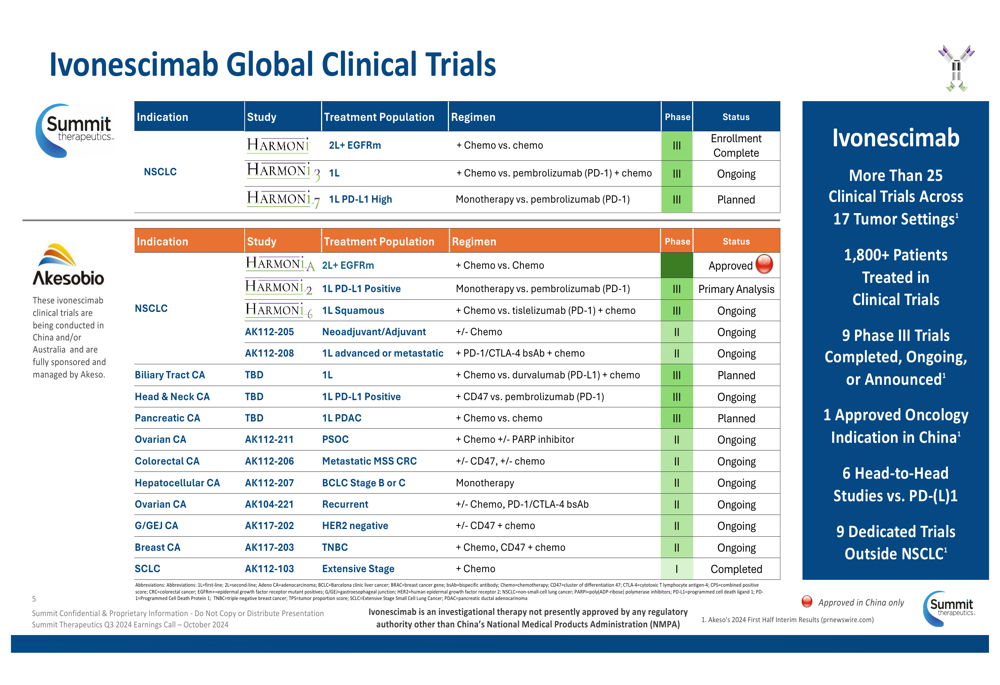
Resultados do estudo HARMONI-2
O destaque mais significativo da apresentação foram os resultados positivos do estudo HARMONI-2, um estudo de Fase III patrocinado pela Akeso comparando ivonescimab com pembrolizumab em pacientes com NSCLC avançado ou metastático PD-L1-positivo. O estudo demonstrou uma melhora estatisticamente significativa na sobrevida livre de progressão com ivonescimab.
Como mostrado na seguinte curva de Kaplan-Meier, o ivonescimab alcançou uma PFS mediana de 11,14 meses em comparação com 5,82 meses para pembrolizumab, representando uma redução de 49% no risco de progressão da doença (HR 0,51, p<0,0001):
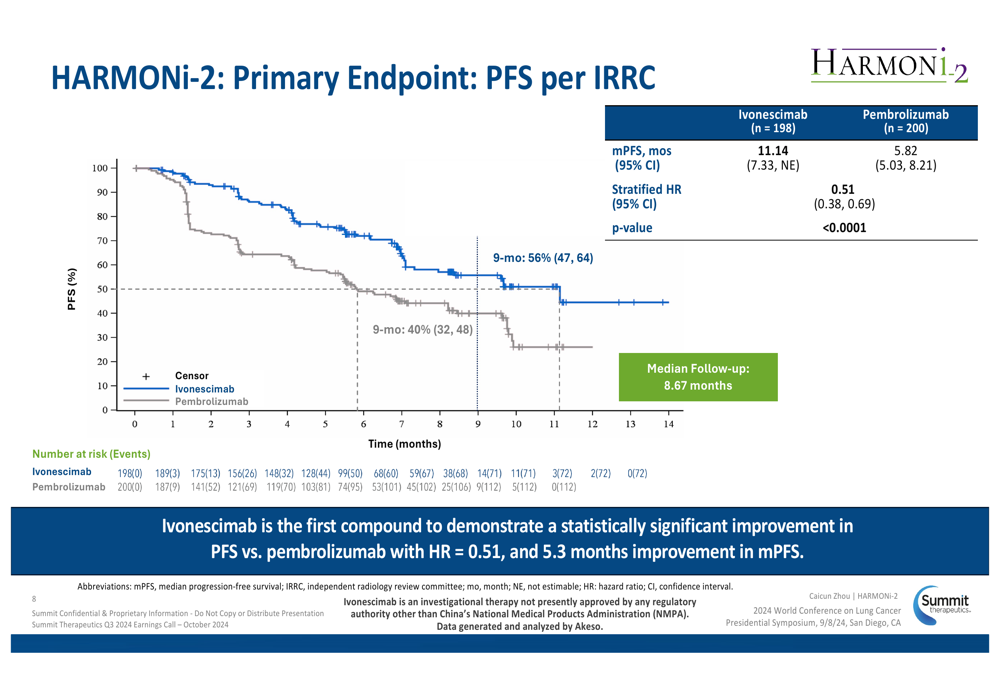
O benefício do ivonescimab foi consistente em todos os subgrupos-chave de pacientes, incluindo aqueles com expressão baixa e alta de PD-L1, bem como histologia escamosa e não-escamosa. As seguintes análises de subgrupos ilustram ainda mais o amplo perfil de eficácia:
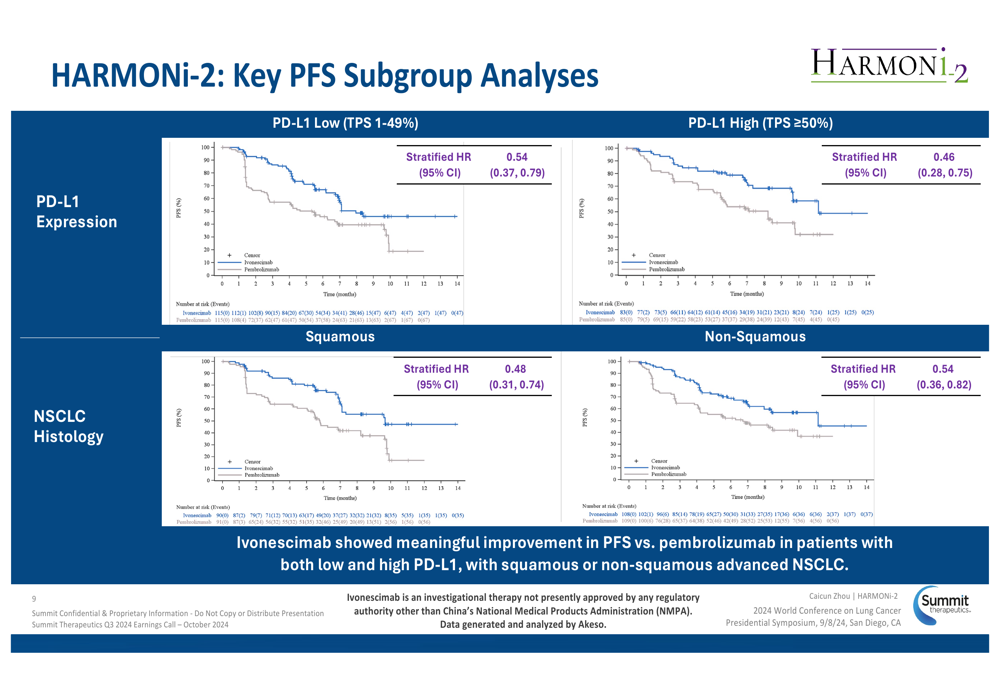
Embora demonstrando eficácia superior, o ivonescimab apresentou um perfil de segurança gerenciável, porém com maior incidência de eventos adversos relacionados ao tratamento (TRAEs) de Grau≥3 em comparação com pembrolizumab (29,4% vs. 15,6%). Os TRAEs mais comuns incluíram proteinúria, aumento da aspartato aminotransferase, hipercolesterolemia, aumento da bilirrubina sanguínea e hipertensão.
O gráfico a seguir detalha a comparação do perfil de segurança entre ivonescimab e pembrolizumab:
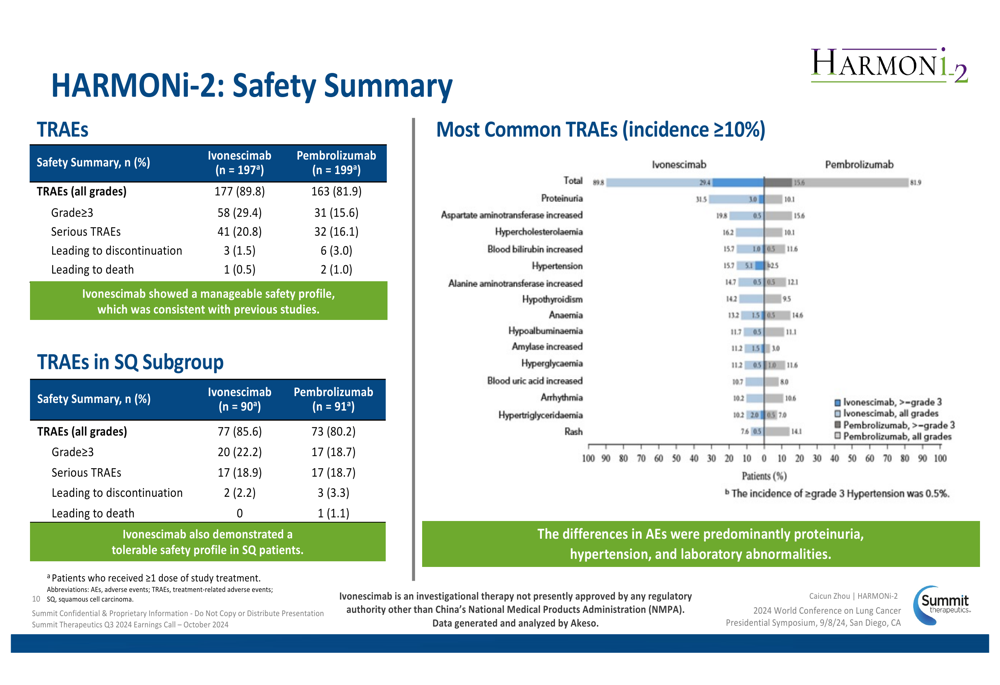
Expansão do programa clínico
Com base nos resultados positivos do HARMONI-2, a Summit está expandindo seu programa de desenvolvimento clínico. A empresa concluiu o recrutamento no estudo global HARMONI de Fase III, com dados preliminares esperados para meados de 2025. Além disso, o estudo HARMONI-3 foi expandido para incluir pacientes com histologia não-escamosa além de tumores escamosos.
A Summit também anunciou planos para iniciar o estudo global HARMONI-7 de Fase III no início de 2025, que comparará a monoterapia com ivonescimab versus monoterapia com pembrolizumab em pacientes com NSCLC com alta expressão de PD-L1 (TPS ≥ 50%).
O design do próximo estudo HARMONI-7 está descrito no slide a seguir:

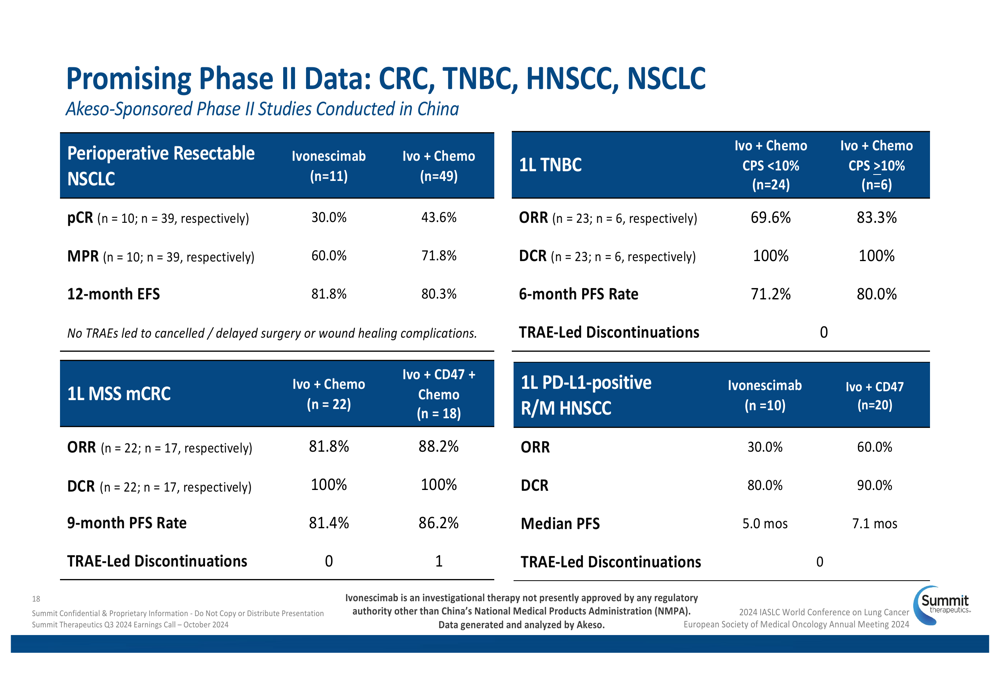
Além do NSCLC, a Summit apresentou dados promissores de Fase II para o ivonescimab em múltiplos tipos de câncer, incluindo câncer colorretal (CRC), câncer de mama triplo-negativo (TNBC), carcinoma de células escamosas de cabeça e pescoço (HNSCC) e NSCLC em estágio inicial. Esses resultados apoiam o potencial para um desenvolvimento clínico mais amplo do ivonescimab em várias indicações oncológicas.
O slide a seguir resume os dados encorajadores de eficácia desses estudos de Fase II:
Desempenho financeiro
Para o 3º tri de 2024, a Summit reportou despesas operacionais totais GAAP de US$ 58,1 milhões, ligeiramente abaixo dos US$ 59,8 milhões no 2º tri de 2024. As despesas de pesquisa e desenvolvimento aumentaram para US$ 37,7 milhões, de US$ 30,8 milhões no trimestre anterior, refletindo o investimento contínuo da empresa em seus programas clínicos. As despesas gerais e administrativas também aumentaram para US$ 20,4 milhões, de US$ 14,0 milhões.
A posição financeira da empresa permanece forte, com US$ 487 milhões em caixa, equivalentes de caixa e investimentos de curto prazo em 30 de setembro de 2024, após a conclusão de uma rodada de financiamento privado de US$ 235 milhões. Com uma capitalização de mercado de US$ 16,1 bilhões, a Summit parece bem posicionada para financiar seus ensaios clínicos em andamento e planejados.
Declarações prospectivas
Olhando para o futuro, a Summit Therapeutics está focada em avançar seu programa de desenvolvimento clínico para o ivonescimab. Os principais marcos futuros incluem:
1. Dados preliminares do estudo global HARMONI de Fase III esperados para meados de 2025
2. Início do estudo global HARMONI-7 de Fase III no início de 2025
3. Exploração contínua do ivonescimab em indicações adicionais de câncer além do NSCLC
A forte posição de caixa da empresa proporciona recursos para perseguir essas iniciativas enquanto mantém flexibilidade operacional. Com o ivonescimab já aprovado na China pela Administração Nacional de Produtos Médicos (NMPA) e mostrando resultados promissores em estudos globais, a Summit está se posicionando como um player significativo no espaço oncológico, particularmente no tratamento de NSCLC.
Embora os dados clínicos apresentados sejam encorajadores, os investidores devem observar que o ivonescimab ainda é uma terapia investigacional não aprovada por autoridades regulatórias fora da China, e resultados adicionais de ensaios clínicos serão críticos para o sucesso de longo prazo da empresa.
Essa notícia foi traduzida com a ajuda de inteligência artificial. Para mais informação, veja nossos Termos de Uso.
Apresentação completa:
